Onlangs zijn er afspraken gemaakt over het medicijn tafamidis bij de behandeling van ATTR-amyloïdose. Deze belangrijke overeenkomst tussen zorgverleners en het Zorginstituut biedt patiënten meer duidelijkheid over hoe en wanneer tafamidis wordt ingezet.
De overeenkomst is onder andere te danken aan twee cardiologen uit onze Medische Adviesraad, dr. Michelle Michels (Erasmus MC) en dr. Christian Knackstedt (Maastricht UMC), en twee betrokken patiënten vanuit Amyloïdose Nederland, John Rusman en Dorien Müller. Naast de twee cardiologen uit onze adviesraad waren nog twee cardiologen betrokken: prof. dr. Peter van der Meer (UMCG) en dr. Marish Oerlemans (UMCU).
Wat betekent de overeenkomst voor patiënten met amyloïdose? Dr. Bouke Hazenberg, voormalig universitair docent in Groningen en reumatoloog in het UMC te Groningen, is gespecialiseerd in de diagnostiek en behandeling van patiënten met amyloïdose. Hij legt uit wat het medicijn doet, en hoe de werking ervan is ontdekt.
Stabilisator
Wat doet tafamidis bij behandeling van ATTR-amyloïdose? En kan het medicijn ook worden toegepast bij andere typen amyloïdose?
Bouke Hazenberg: “Tafamidis is een TTR tetrameer-stabilisator. Transthyretine (TTR) is een tetrameer: het bestaat uit vier gelijke delen (monomeren) die aan elkaar geschakeld zijn zodat ze samen een tunneltje vormen. In dat tunneltje passen twee schildklierhormoon-moleculen, die zo worden getransporteerd in de bloedbaan. Die vier monomeren zitten niet al te stevig aan elkaar verbonden en kunnen van elkaar losraken. Als sprake is van een mutatie in het TTR-eiwit, dan zitten de monomeren meestal nog minder goed aan elkaar vast. In die situatie kan de tetrameer gemakkelijk uit elkaar vallen en komen er meer monomeren beschikbaar. Vooral als er een mutatie is, willen de monomeren wel aan elkaar plakken, maar in een andere vorm en veel steviger. Die zogeheten [cursief]aggregatie van monomeren[/cursief] is het begin van de vorming van een amyloïdfibril (vezel). Als dat eenmaal begonnen is, blijft het doorgaan bij ATTR-amyloïdose.
Een tetrameer-stabilisator, zoals tafamidis, hecht zich in het tunneltje vast aan alle vier monomeren, verbindt ze steviger met elkaar en voorkomt zo dat de tetrameer uit elkaar valt. Er komen veel minder monomeren beschikbaar voor de verdere aangroei van het amyloïd, en daardoor wordt de toename van amyloïd met bijbehorende ziekteverschijnselen enorm afgeremd.
Omdat tafamidis, en andere tetrameer-stabilisatoren, zich specifiek binden in het tunneltje van TTR, zijn ze alleen ontworpen en bedoeld voor ATTR-amyloïdose. Ze zijn niet bruikbaar voor alle andere typen amyloïdose.”
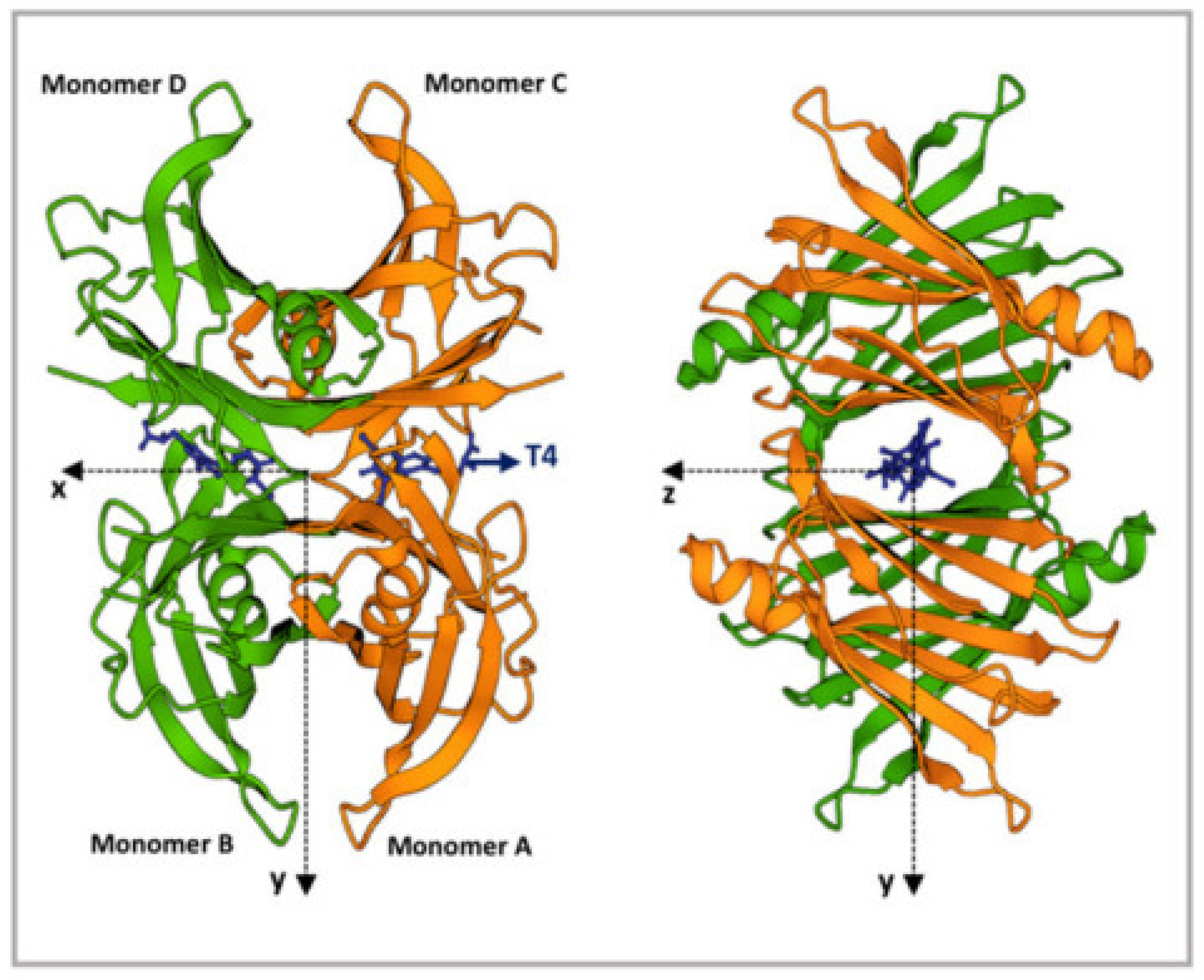
“In de illustratie zijn de vier monomeren te zien die samen een tetrameer vormen. Deze afbeelding beeldt dit helder uit in twee richtingen, waardoor het tunneltje (met daarin T4, wat het schildklierhormoon is) mooi zichtbaar is.”
Ontdekking
Wanneer is gebleken dat tafamidis gunstig werkt bij de behandeling van ATTR?
“De slimme Californische biochemicus Jeff Kelly kwam in 2003 op het idee om de TTR-tetrameer te stabiliseren. Een bestaand medicament, de pijnstiller diflunisal, had zo’n werking. Ook een ander medicijn leek geschikt te zijn en dat was tafamidis. Negen jaar later, in 2012 werd in een internationaal experiment, het eerste bewijs geleverd dat een dagelijkse dosis van 20 mg tafamidis een gunstig effect had op polyneuropathie (zenuwschade in de ledematen] bij erfelijke ATTR-amyloïdose. Het bewijs voor diflunisal, tweemaal daags 250 mg, volgde al in 2013.
Het tweede bewijs van de werkzaamheid van een dagelijkse dosis van 80 mg tafamidis (61 mg in een iets andere samenstelling), maar nu op de [cursief]cardiomyopathie[/cursief] (verdikte spieren in de wand van het hart) bij ATTR-amyloïdose, werd in 2018, 15 jaar na Kelly's eerste idee, geleverd in een volgend internationaal proefonderzoek.”
Wat er verandert
Hoe werd tafamidis tot nu toe toegepast, en wat wijzigt er door deze overeenkomst?
“De meest doeltreffende toepassing was al goed beschreven voor de behandeling van polyneuropathie, maar nog niet van cardiomyopathie, en dankzij dit document nu wel. Omdat tafamidis een erg duur medicijn is, € 366 per tablet of capsule wat kan oplopen tot € 133.000 per jaar, wil de overheid dat het alleen beschikbaar is voor mensen die er baat bij hebben. En dus niet wordt voorgeschreven aan mensen die het (nog) niet nodig hebben of die er überhaupt geen baat (meer) bij hebben. Het medicijn wordt volledig vergoed door zorgverzekeraars. Daarbij wil de overheid gebruik maken van de amyloïdose-expertisecentra en de daarmee samenwerkende behandelcentra, om goed inzicht te krijgen in de aantallen en het ziektebeloop van de betrokken patiënten.
Daarnaast bewaken de expertisecentra de diagnostiek (welke mensen komen voor tafamidis in aanmerking) en de behandeling (wanneer beginnen, hoelang voortzetten) met follow-up (monitoren van bijwerkingen en of de ziekteverschijnselen stabiliseren, toch toenemen of juist veranderen).
Ook deelname aan wetenschappelijk onderzoek en toepassen van nieuwe medicamenten hoort bij dit expertisenetwerk. Deze overeenkomst moet voorkomen dat individuele neurologen en cardiologen zonder zicht op de volledige problematiek van de patiënt, een peperduur medicament kunnen voorschrijven.”
Geldverspilling tegengaan
Waarom is deze overeenkomst belangrijk? En, behalve voor de patiënt, voor wie nog meer?
“Gepast gebruik leidt tot goede patiëntenzorg waarbij geldverspilling wordt tegengegaan. Patiënten die baat bij het middel kunnen hebben komen in aanmerking. Expertisecentra bewaken het diagnose- en behandeltraject en zijn aanspreekpunt voor de overheid. De overeenkomst wordt onderdeel van een groter zorgpakket binnen het expertisenetwerk, waar ook andere dure medicamenten hun plaats kunnen krijgen. Doel is en blijft dat iedere patiënt de best passende zorg en medicatie krijgt.”
Start- en stopcriteria
Wat zijn de belangrijkste afspraken in de overeenkomst?
“De belangrijkste afspraak betreft de startcriteria voor behandeling met 61 mg tafamidis per dag. Daarnaast zijn er afspraken over
- het vervolgen van de behandeling via multidisciplinair overleg binnen het expertisenetwerk.
- Jaarlijkse evaluatie van het resultaat van de behandeling binnen het expertisecentrum
- met zo nodig tussentijdse controles in het verwijzend centrum.
- En naast de startcriteria zijn ook stopcriteria afgesproken. Tafamidis wordt gestopt in geval van ernstig hartfalen, ondanks optimale behandeling. Datzelfde geldt als sprake is van een beperkte levensverwachting (bijvoorbeeld door bijkomende andere ernstige kwalen). En ook als er sprake zou zijn van ernstige bijwerkingen van tafamidis (tot nu toe nog niet beschreven).”
Meer duidelijkheid
Welke verbeteringen kan een patiënt verwachten?
“Vooral meer duidelijkheid. Behandelaars die met de patiënt en met elkaar goede afspraken maken, heldere overlegstructuren en goed omlijnde criteria voor diagnostiek, behandeling en follow-up.”
De overeenkomst ‘Gepast gebruik arrangement tafamidis’ kunt u vinden op de website van Zorginstituut Nederland.